Question n°3 : mélange réfrigérant
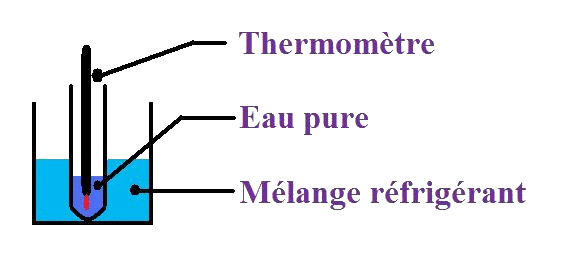
La glace fond à 0°C, c’est ce que l’on apprend à l’école...
Ce n’est pas le cas de l’eau salée ! En effet le mélange eau + sel devient solide qu’à une température plus basse. Lorsqu’on réalise mélange de glace et de sel, la température chute en dessous de zéro.
Le mélange glace + sel peut être liquide, mais a besoin d’énergie pour le devenir !
L’énergie thermique interne du système diminuant , la température qui n’est qu’une mesure de cette énergie chute également.
Ceci est bien connu des poissonniers puisqu’ils exposent leur marchandise sur ce mélange de glace pilée et de gros sel.
Nous pouvons vérifier expérimentalement que la température de solidification d’une eau salée est d’autant plus basse que sa concentration en sel est plus élevée. Les canadiens constatent souvent en hiver que le fleuve Saint-Laurent (eau douce) gèle à son embouchure alors que la mer (environ 35 g de sel par litre) ne gèle pas à une température de - 2°C
Les service de la D.D.E. répandent, lorsqu’il gèle en hiver, du sel souvent mélangé à du sable sur les routes à titre préventif, avant l’apparition du verglas ou de la neige, ou curatif après leur apparition. Ce traitement est efficace tant que la température ne descend pas en dessous de - 7°C. Pour des températures plus basses il faudrait utiliser du chlorure de calcium bien plus cher.
Les anciens qui ne possédaient pas de congélateur fabriquaient glaces et sorbets en entourant le récipient du mélange réfrigérant (un tiers de sel pour deux tiers de glace pilée) pouvant atteindre une température de - 15°C
Le mélange réfrigérant, dans lequel la glace fond et le sel se dissout, prend de la chaleur à la crème ou jus sucré permettant leur solidification mais aussi à l’air ambiant contenant de la vapeur d’eau formant du givre sur les parois du récipient.
